Ammoniak
| Strukturformel | |||
|---|---|---|---|

| |||
| Allgemeen | |||
| Naam | Ammoniak | ||
| Annere Naams | Azan; R717 | ||
| Summenformel | NH3 | ||
| CAS-Tall | 7664-41-7 | ||
| Kortbeschrieven | Gas ahn Klöör mit steken Röök | ||
| Egenschoppen | |||
| Molar Masse | 17,03 g·mol–1 | ||
| Phaas | gasförmig | ||
| Dicht | 0,7714 kg·m–3 (0°C, 1013 mbar)[1] | ||
| Smöltpunkt | –77,7 °C (5,3 bar)[1] | ||
| Kaakpunkt | –33 °C[1] | ||
| Dampdruck | 8,5737 bar[1] (20 °C) | ||
| pKS-Weert | |||
| Löslichkeit |
541 g/l bi 20 °C in Water[1]; goot lööslich in Alkohol, Aceton, slecht in Hexan | ||
| Sekerheitshenwiesen | |||
| Gefahrstoffkennteken ut RL 67/548/EWG, Anh. 1 | |||
|
| |||
| R- un S-Sätz | R: 10-23-34-50 | ||
| S: (1/2)-9-16-26-36/37/39-45-61 | |||
| Wietere Sekerheitshenwiesen | |||
| MAK | 14 mg·m–3[1] | ||
| Thermodynaamsch Egenschoppen | |||
| ΔHf0 |
−46,1 kJ·mol−1[4] | ||
| Sowiet mööglich un tyypsch, warrt dat SI-Eenheitensystem bruukt. Wenn nich anners anmarkt, gellt de angeven Daten bi Standardbedingen. | |||
Ammoniak is en cheemsch Verbinnen ut Stickstoff un Waterstoff mit de Summenformel NH3. De Naam is afleidt vun’t Ammonsolt (Ammoniumchlorid) ut de Ammonsoaas, de vundaag Oaas Siwa nöömt warrt. Ammoniak is en gitfig Gas ahn Klöör mit en Röök, de düchtig in de Nees stickt, de Ogen to Tranen reizt un sticken wirkt. Ammoniakgas hett en lüttere Dicht as de Luft. Bruukt warrt das Gas bi’t Herstellen vun Düngemiddels, Farvstoffen un Sprengstoff. Ammoniak is butendem en Base, de sik goot in Water lösen lett un denn Salmiakgeist (Ammoniumhydroxid) billt. Ammoniakgas warrt mit de UN-Tall 1005 betekent, de waterige Lösen hett de UN-Tall 2672.
Annere Egenschoppen
[ännern | Bornkood ännern]| kritische Temperatur | 132,5 °C |
| kritisch Druck | ruchweg 11,3 MPa (Megapascal) |
| pKb | 4,75 |
| Smöltwarms | 5,655 kJ/mol (bi −77 °C) |
| Verdampensenthalpie | 22 kJ/mol (bi −33 °C) |
| Lööswarms | 30,5 kJ/mol (bi 25 °C) |
| Warmskapazität cp | 35,6 J/(mol K) bi 298 K |
| thermische Leddanlaag | 0,02494 W/(m K) |
| Schallsnelligkeit | 414 m/s |
Ammoniak löst sik bannig goot in Water: Bi 0 °C löst sik in 100 ml Water 90,7 g (≙ 120 l). De Lösen, de dorbi tostannen kummt, warrt as Salmiakgeist (Ammoniumhydroxid) betekent. Se reageert alkaalsch.
Mischen ut Ammoniakgas und de Luft künnt in’t Rebeet vun 15,5 bit 30 Volumenprozent Ammoniak explodeeren. An hitte Böverflachen af 630 °C kann dat Gas in Stickstoff un Waterstoff verfallen. Disse Verfallsreakschoon warrt dör Metallen katalyseert, so dat de Verfall in groottechnische Anlagen ok al af 300 °C vörkamen kann, wat de Mööglichkeit vun en explosiven Verfall bargt. Ammoniak verbrennt gau un vullstännig, so dat dorna keen NH3 mehr fasttostellen is.
Op fuchtige Böverflachen hat Ammoniak en ätzen Wirken. Sünners fuchtige Huut, Sliemhhüüt, Lungen un Ogen warrt dorüm licht verätzt. Wenn Ammoniak slaken warrt, löst dat blödig Spucken ut mit gresige Wehdaag. Bi’t Inaten maakt dat Schaden an de Lung, wat ünner swore Ümstännen bit to’n Dood föhren kann. En Ammoniakandeel in de Luft vun 0,5 % wirkt na 30 bit 60 Minuuten döödlich.
Süür-Basen-Egenschoppen
[ännern | Bornkood ännern]Ammoniak is amphoter, dat heet dat dat as Base un as Süür reageeren kann. As Base billt Ammoniak ünner Protoneeren ionische Ammoniumsolten, as Süür billt dat mit starke Basen ünner Deprotoneeren ionische Amiden. Ut dissen Grund besteiht in fletig Ammoniak en Autoprotolysgliekgewicht, dat dör en Ionenprodukt beschreven warrn kann:
Struktur
[ännern | Bornkood ännern]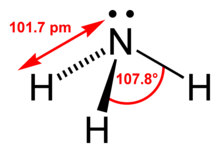

Dat Ammoniak-Molekül is nich even, man hett de Form vun en dreesietige Pyramid (trigonal-pyramidal). De Struktur leidt sik vun’n Tetraeder af, in den dat fre’e Elektronenpoor vun’t Stickstoff, dat also nich an Binenn bedeeligt is, een Eck besetten deit. As sik de Ladungen afstöten doot twüschen de N-H-Binnelektronen un dat fre’e Elektronenpoor vun’n Stickstoff, dat ok Ruum innimmt, leegt de dree Waterstoffatomen nich mit dat Stickstoffatom op de glieek Even. Op disse Wies sünd de Binnelektronen un dat fre’e Poor mööglichst wiet vunenanner weg.
Dat Molekül is polariseert, vun wegen dat de Stickstoff en högere Elektronegativität hett as de Waterstoff un dat Molekül anwinkelt is: In de Neeg vun dat fre’e Elektronenpoor liggt dorüm en högere negative Ladungsdicht vör. Dat is dorüm de Steedwoneem Elektrophilen as to’n Bispeel H+ vör allen angriept. Bi Ruumtemperatur is dat Ammoniakmolekül nich stief. Dat fre’e Elektronenpoor kann sik op de gegenöverliggen Siet verlagern, wobi de Waterstoffmolekülen denn ok op de annere Siet utwieken doot. Dordör kummt dat to en „Dörswingen“ vun’t Molekül, wat sik verglieken lett mit dat Ümklappen vun en Regenschirm. Disse Egenschop hebbt ok de Verbinnen, de vun’t Ammoniak afleidt sünd as t. B. de Aminen, so lang se nich dör en stieve Geometrie vun’t Restmolekül an’t „Dörswingen“ hinnert warrt.
Nawies
[ännern | Bornkood ännern]To’n Nawies vun Ammoniak reckt dat faken al ut, en vörsichtige Röökproov to maken. Lütte Gasmengden künnt to’n Bispeel mit ’n beten fuchtig Indikaterpapeer nawiest warrn, dat op de OH−-Ionen, de ut dak Ammoniak un dat Water entstaht, mit en Farvreakschoon antert. En fotometrisch Verfohren is de Reakschoon vun Ammoniak mit Tetraiodomercurat to en orangeklöörte Verbinnen (Nessler-Reakschoon) oder mit Koppersulfatlösen to den deppblauen Koppertetraamminkomplex (Komplexbillnreakschoon). Bi en tweet fotometrisch Verfohren billt Ammoniak mit Hypochlorit-Ionen Chloramin, wat mit Phenolen klöörte Indophenolen billt. Disse Nawies warrt as Indophenolreakschoon oder Berthelot-Reaktschoon betekent.
Herstellen
[ännern | Bornkood ännern]In’n industriellen Rahmen warrt hüüt de wiet gröötste Deel (ca. 90 % vun de Weltprodukschoon) ut Waterstoff un Stickstoff na dat Haber-Bosch-Verfohren herstellt.
Alternativ kann Ammoniak ut Kalkstickstoff wunnen warrn (Kalkstickstoffverfohren vun Rothe-Frank-Caro)
oder dör Hydrolys vun Nitriden (Serpek-Verfohren)
En technische Bedüden hebbt de beiden Verfohren aver nich, as Synthees na de Haber-Bosch-Methood billiger is.
En annern Weg NH3 to tügen is de Redukschoon vun Stickstoffmonoxid (NO) mit Waterstoff (H2):
Bito kann man dat Gas ok mit Natronlaug ut Salmiaksolt (Ammoniumchlorid) rutlösen (Verdrängreakschoon, is gliektietig en Nawiesreakschoon för Ammoniumsolten):
Bruuk un anners wat
[ännern | Bornkood ännern]Ammoniak is een vun de wichtigsten un fakensten Produkten vun de cheemschen Industrie. De Produkschoon vun Ammoniak weltwiet bedriggt vundaag ruchweg 125 Millionen Tunnen. Ungefähr dree Prozent vun de weltwiet produzeerten Energie warrt för de Herstellen vun Ammoniak verbruukt. De gröttste Deel dorvun deent as Utgangsstoff för Stickstoffdünger. Annere Anwennen vun Ammoniak sünd:
- Ammoniakmolekülen weern 1949 för den Bedrief vun de eersten Atomklocken bruukt.
- Herstellen vun Sprengstoffen.
- Fletig Ammoniak warrt wegen sien hoge Verdampenswarms in Küllmaschienen ünner de Küllmiddel-Beteken R717 insett.
- Bi’t Textilvereddeln, to’n Plastifizeeren vun Holt un as nichwaterig Löösmiddel.
- Ammoniakgas warrt as Destrakschoonsmiddel bruukt.
- In waterfre’e fletige Form as Reagenz un Löösmiddel för de Birch-Reakschoon in de orgaansch-cheemschen Synthees.
- In de Metallindustrie as Ammoniak-Splittgas för de Nitreerharden un as Schuulgas för de Warmsbehanneln, ok to’n Blankgleihn.
- As Ammoniakwater to’n Beizen un Saubermaken. Dat warrt insett to’n Utschalten vun Chlor un Formaldehyd na Desinfekschoonsbehanneln.
- To’n Entsweveln vun Rookgas. Dorbi billt sik Ammoniumsulfat, dat as Düngemiddel bruukt warrt.
- Kunzentreert Ammoniak (ca. 35 % in Water) weer lange Tiet to’n Entwickeln vun Lichtpausen verwennt.
- För’t SCR-Verfohren bi’t Rookgasreinigen vun Kraftwarken un bi’t Saubermaken vun Afgas bi Dieselmotoren.
- In Dampkraftwarken un annere Dampsystemen as Korrosionsinhibiter dör’t Alkaliseeren vun Kondensat un Water. Goot is dorbi, dat Ammoniak anners as annere Alkaliseermiddels ok in de Dampphaas övergeiht un so ok de Dampleitungen schuult.
- To’n Herstellen vun Heelmiddels.
- To’n Proven vun de Dichtheit vun Chlorgasanlagen. Bi Lecks kummt dat dör dat Ammoniumchlorid, wat dorbi entsteiht, to’n Billn vun Nevel.
- In Fletige oder överkritische Phaas kriggt dat jümmer mehr Bedüden as Löösmiddel, dat nich oxideert, ünner annern wegen sien physikaalsch-cheemschen Gliekheit to Water (Waterstoffbrüchenbinnen, Egendissoziatschoon2 NH3 → NH4+ + NH2−, usw.)
- In’n Magen warrt Ammoniak vun’t Bakterium Helicobacter pylori mit Help vun’t Enzym Urease ut Harnstoff herstellt, üm de Magensüür to neutraliseeren un dormit in’n Magen överleven to künnen. Dit Bakterium is de fakenste Oorsaak för Magengeswüren.
- Ut Ammoniak warrt tallrieke wietere Vörprodukten herstellt. Dorünner sünd vör allen vun Bedüden:
Ammoniak
_________|_________________________________
| | |
Oxidatschoon | | sämtlich
| (NH2)2CO (Harnstoff) wietere
| / \ orgaansch
Salpetersüür Kunsthorzen \ un
/ / | | \ Düngemiddel anorgaansch
Nitraten / | | \ Stickstoff
/ | | \ / / | \
Düngemiddel / | \ Hydroxylamin / | Nitrilen
/ | Nitroaromaten / |
/ Adipinsüür \ Aminen Hydrazin
Sprengstoffen Anilin(-derivaten)
Borns
[ännern | Bornkood ännern]- ↑ a b c d e f Indrag to Kohlenstoffdioxid in de GESTIS-Stoffdatenbank vun’t BGIA; Afropen an’n 28.6.2008
- ↑ Christen, Meyer: Grundlagen der allgemeinen und anorganischen Chemie. Diesterweg, 1997, ISBN 978-3793554936.
- ↑ Frederick G. Bordwell, George E. Drucker und Herbert E. Fried: Acidities of Carbon and Nitrogen Acids: The Aromaticity of the Cyclopentadienyl Anion, in: J. Org. Chem. 1981, 46, 632-635 doi:10.1021/jo00316a032
- ↑ PAETEC Formelsammeln Utgaav 2003, Siet 116
Literatur
[ännern | Bornkood ännern]- Robert Schlögl: Katalytische Ammoniaksynthese - eine „unendliche Geschichte“? Angewandte Chemie 115(18), S. 2050–2055 (2003), ISSN 0044-8249
Weblenken
[ännern | Bornkood ännern]- Ümweltberaaten: Ammoniak un Ammonium
- Ammoniak-Springbrunnen Versöök to’n Nawies vun de rutragen Waterlöslichkeit: Anleiden un Video







